ICH Q10における医薬品品質システム
ICH Q10における医薬品品質システムの基本構造と経営層の責任
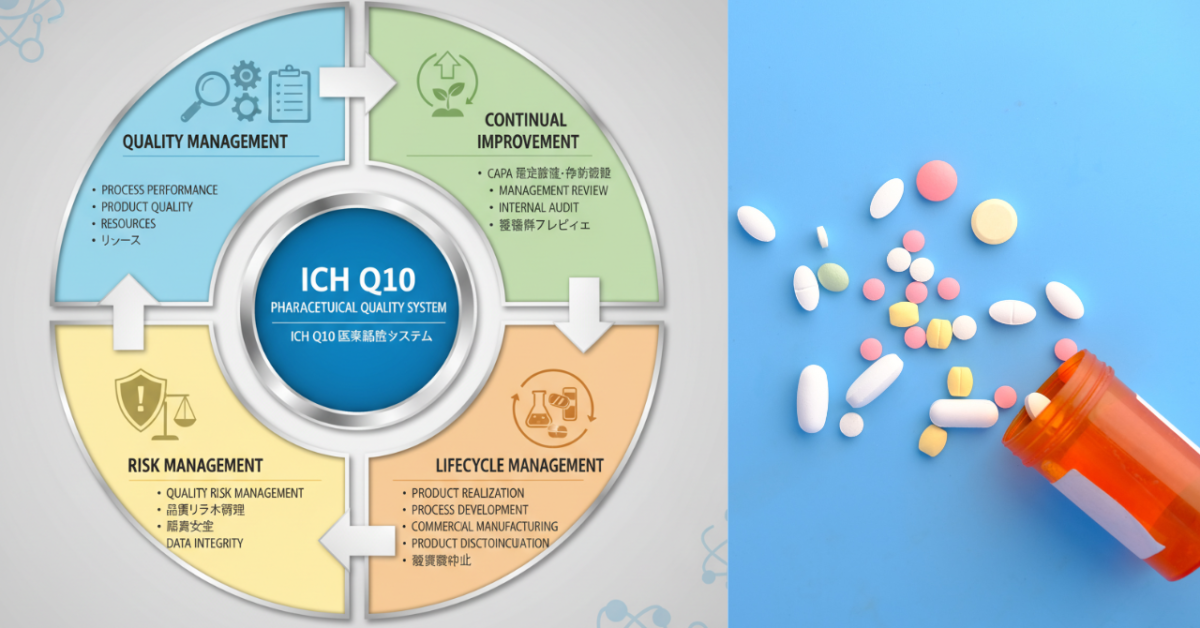
医薬品業界における品質保証は、患者の安全と有効性を確保するための最も重要な要素の一つである。国際共同会議(ICH)が策定した「ICH Q10:医薬品品質システム(PQS)」は、国際的な規制基準として広まり、製薬企業の品質管理活動の共通指針となっている。本稿では、ICH Q10で定義される4つの主なシステム要素と、それらの相互関係、さらに経営層の役割について解説する。
ICH Q10の概要とPQSの意義
ICH Q10は、開発から製造に至るライフサイクル全体にわたり、一貫した品質を維持・向上させることを目的としたガイダンスである。このガイダンスは、法規制を補完するものであり、企業が自社の医薬品品質を高めるための枠組みを提供する。本指針に従うことで、製品の信頼性や規制遵守の強化に寄与するのが大きな特徴である。
四つの柱:ICH Q10の主要要素
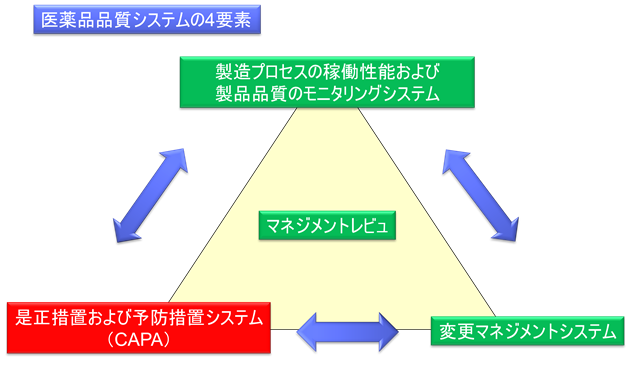
ICH Q10が中心に据える医薬品品質システムは、以下の4つの要素で構成される。
1. モニタリング
モニタリングは、製造プロセスおよび品質に関するパラメータを継続的に監視・評価する活動である。製品や工程の変動や異常を早期に検知し、問題の予兆をとらえることによって、継続的な改善や品質リスクの低減につながる。
2. CAPA(是正措置・予防措置)
CAPA(Corrective and Preventive Action)は、品質問題の原因究明と、その再発防止または未然防止のための施策を意味する。発生した問題を単に修正するだけではなく、根本原因に基づき再発防止策・予防策を講じることが重要である。
3. 変更管理
変更管理とは、製造方法、設備、原材料などに対して行われる変更を適切に評価・承認し、管理する仕組みを指す。適切な変更管理を実施することで、品質へのリスクを未然に防ぎつつ、継続的な改善活動を推進できる。
4. マネジメントレビュー
マネジメントレビューは、経営層を含む組織の要職者が品質システム全体の有効性や適合性を定期的に評価し、方針や資源の見直しを行う活動である。この活動は、組織全体としての品質保証を高次元に保つために不可欠である。
四要素の相互関係
これら四つの要素は、単独で機能するものではなく、相互に連携しあうことで品質システムの強固な基盤を形成している。例えば、モニタリングによって検知された変動や異常は、CAPAへとフィードバックされ、必要に応じて変更管理に進展する。これら一連の活動の成果や課題は、マネジメントレビューで統括的に評価され、全社的な品質改善へとつながる。そのため、これら全要素が有機的に連動することが、品質保証体制の堅牢化と継続的改善の達成に不可欠である。
経営層の責任とリーダーシップ
ICH Q10では、品質の維持・向上において経営層の積極的な関与とリーダーシップが強調されている。経営層は単に指示を出す存在ではなく、品質目標の設定、資源の確保、継続的改善活動の推進に責任を持つ必要がある。また、マネジメントレビューを通じて品質システムの現状を的確に把握し、組織全体に品質文化を根付かせることが求められる。これにより、組織は規制要求のみならず、企業としての信頼性や社会的責任をより高い水準で達成できる。
おわりに
ICH Q10の医薬品品質システムは、4つの要素が有機的に連動し、経営層の主体的な関与によって高次元の品質保証が実現される枠組みである。医薬品企業にとって、これらの要素とその相互関係、そして経営層の責任を正しく理解し実践することが、医薬品品質の維持・向上と持続的な成長に直結する。本稿が、初心者を含めた業界関係者の理解深化の一助となれば幸いである。








