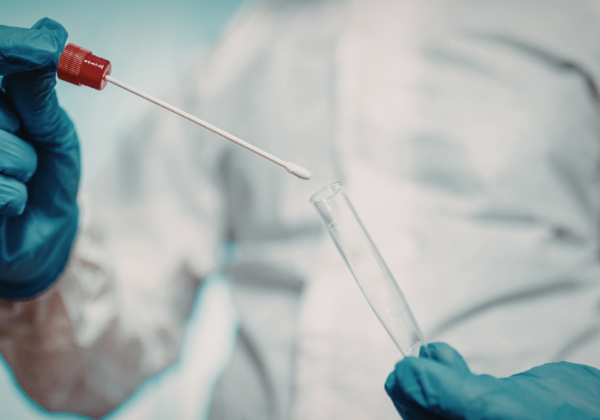
IVDのリスクモデルの特殊性
体外診断用医療機器(IVD)のリスクモデルの特殊性とは何か 医療機器と聞くと、多くの人は手術器具やペースメーカーなど、患者の体に...

体外診断用医療機器(IVD)のリスクモデルの特殊性とは何か 医療機器と聞くと、多くの人は手術器具やペースメーカーなど、患者の体に...

リスクマネジメントの現場で働く者なら誰もが直面する根本的な問いがある。「なぜ危害の重大性を下げることは難しく、発生確率を下げるこ...

リスクマネジメントファイルのサンプルはこちら。 医療機器の開発において、安全性の確保は最重要課題である。しかし、開発プロセスで生...
医療機器の開発・製造において、「医療機器ファミリー」という概念は、安全性確保と業務効率化の両面から極めて重要な役割を果たしている...

医療機器や医薬品の開発において、「完全に安全」な製品を作ることは現実的に不可能である。どんなに優れた製品であっても、何らかのリス...

人気のセミナーがビデオになって販売中!
社内研修用・自習用教材が欲しい方にオススメ!

医療機器ソフトウェアの開発において、IEC62304規格はソフトウェア開発の各段階で作成される成果物に対して検証活動を実施し、そ...

SaMDとは何か – 単体プログラムが医療機器になる時代 スマートフォンアプリが医師の診断を支援し、ゲームのようなソ...

医療機器や産業機器の設計において、「合理的に予見可能な誤使用」という概念は、製品の安全性を確保する上で極めて重要である。製造業者...

医療機器のリスクマネジメントにおいて、リスクの定義は、リスク = 危害の発生確率 × その危害の重大性である。ここで注意が必要な...

製品の安全性を確保することは、メーカーにとって最も重要な責務の一つである。しかし、どのような製品にも必ず何らかのリスクが存在する...

当社VOD配信セミナーは、視聴期間および回数制限はございません。
お好きな時間に、繰り返し何度でもご視聴いただけます。