電子生データの特定とデータインテグリティ確保
電子生データ特定の重要性
データインテグリティを確保する上で最も重要な基盤となるのが、電子生データの特定である。電子記録の特性として、複数回コピーを行っても完全に同一のデータが作成されるため、どのデータが真の生データであるかを特定することは極めて困難である。このような特性を踏まえ、標準操作手順書(SOP)において電子生データの定義を明確に規定することが不可欠となる。
生データの定義と一貫性の維持
生データの定義においては、データが発生する各段階での扱いを具体的に規定する必要がある。例えば、測定機器に接続された温湿度計のSDカードに記録されたデータ、そこからパソコンに取り込まれたデータ、さらにサーバーにバックアップされたデータなど、データライフサイクルの中でどの時点のデータを正式な生データとして扱うかを明確に定める必要がある。この定義は、一度確立された後は恣意的な変更を防ぐため、厳格に維持されなければならない。
生データの管理要件
生データとして定義されたデータには、複数の要件が課される。具体的には、不正アクセスを防ぐためのセキュリティ対策の実施、データの変更履歴を記録する監査証跡の確保、そしてデータ消失を防ぐためのバックアップ体制の整備が必要となる。SDカードなどの可搬型媒体は、これらの要件を十分に満たすことが困難であるため、要件を満たせる適切な電子システムへの移行を検討する必要がある。
タイプライターエクスキューズの問題
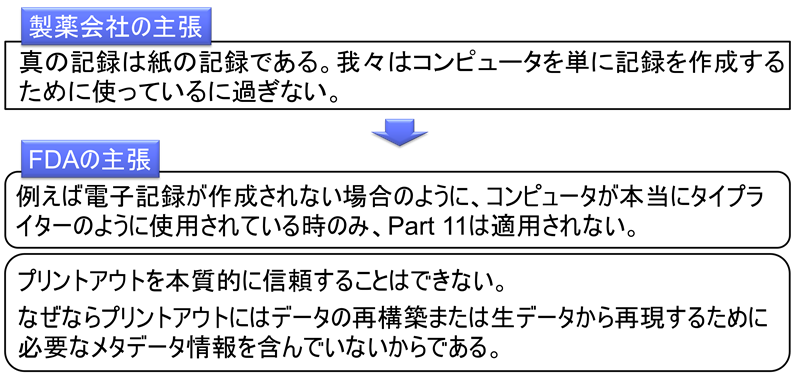
電子記録の管理に関して特に注意すべき点として、「タイプライターエクスキューズ」と呼ばれる考え方がある。これは、電子記録を紙に印刷して署名する際に、コンピュータをタイプライターと同様の単なる印刷装置として扱おうとする考え方である。しかし、この主張は規制当局からは受け入れられない。その理由は、コンピュータとタイプライターの機能的な本質の違いにある。タイプライターでは1回限りの印刷しかできないのに対し、コンピュータでは電子記録を保持し続け、任意のタイミングで何度でも印刷することが可能である。この特性により、査察直前にデータを改ざんして再印刷し、過去の日付で署名するといった不正が技術的に可能となる。
タイプライターイクスキューズ
規制当局の見解
このような観点から、米国食品医薬品局(FDA)は、最終的に紙での管理を行う場合であっても、電子記録を保持している限りはFDA 21 CFR Part 11(パートイレブン)の適用対象となることを明確に示している。日本においても、医薬品等の承認又は許可等に係る申請等における電磁的記録及び電子署名の利用について(ER/ES指針)において、同様の考え方が示されており、国際的に整合した規制の枠組みが形成されている。







