
医療機器の基本要件基準とは
医療機器は人の命や健康に直接関わる製品であるため、その安全性と有効性を確保することが極めて重要である。そのための基盤となるのが「...

医療機器は人の命や健康に直接関わる製品であるため、その安全性と有効性を確保することが極めて重要である。そのための基盤となるのが「...

医療機器規制における医療機器の設計開発においては、医療機器の分類やタイプによって異なる評価要件が適用される。一般医療機器(非IV...

国際標準化機構(ISO)や国際電気標準会議(IEC)は、国際規格を定める主要な機関として、グローバルな産業活動や技術開発の基盤を...

IEC 62304との関係性IEC 81001-5-1:2021は、IEC 62304「医療機器ソフトウェア-ソフトウェアライフ...

FDA QSR (Quality System Regulation)の§820.250は、医療機器の品質保証におけるデータ分析...

医療機器規制において、設計管理、製造管理、購買管理、CAPA、苦情管理、不適合品管理など、非常に煩雑な業務が求められています。
これら業務を効率化し、一元管理す...

救急車内という特殊な環境下で、重篤な患者の命をつなぐために操作される心電図計。救急救命士は極めて限られた時間の中で、正確な診断と...

緊急時における人間の認知・行動特性は、平常時とは大きく異なる。突然の心肺停止に遭遇した場面では、周囲に人が集まり、緊張と焦りの中...
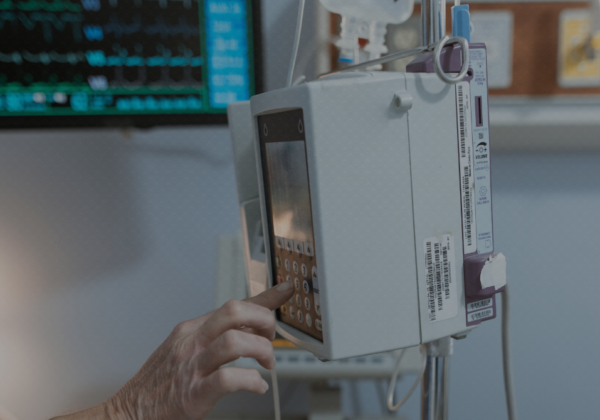
医療現場における機器のユーザビリティは、患者の安全に直結する重要な要素である。ある医療機関で発生した輸液ポンプの誤操作事例は、こ...

1994年4月26日、名古屋空港に着陸態勢に入っていた中華航空140便が墜落し、271名の乗員乗客のうち264名が犠牲となる悲惨...

航空機パイロットとして航空機を操縦するためには、基本的な事業用操縦士資格または定期運送用操縦士資格の取得に加えて、操縦する特定の...

当社VOD配信セミナーは、視聴期間および回数制限はございません。
お好きな時間に、繰り返し何度でもご視聴いただけます。