「Validation」から「Verification」へ
「Validation」から「Verification」へ
今から20年以上も前になるが、2001年12月にGAMP 4が発行された。タイトルは「GAMP Guide for Validation of Automated Systems」であった。
実は、GAMP 4はFDAもレビュに参加した経緯がある。そのため、GAMP 4は当時のCSVのデファクトスタンダードとなった。
しかしながら、大きな問題があった。それは、コンプライアンスコストである。
GAMP 4当時は、サプライヤが実施したテストなどの活動を、製薬企業が繰り返すといった、二重の品質保証を実施していたためである。
企業が使用したコンプライアンスコストは、そのまま製品の価格に転嫁され、最終的には患者負担となってしまうのである。
ASTM E2500
そこでFDAは、製薬業界とは縁もゆかりもないASTM(American Society for Testing and Materials)という団体に、新しい医薬品製造装置のテストに関するガイドラインの策定を委託したのである。
ASTMは、材料、製品、システム、サービスに関する試験方法、標準、規格を開発している。世界100ヶ国以上にメンバーを擁している。ASTMが開発した試験方法や標準は、製品の安全性、品質、性能を保証するために、世界中の企業や政府機関で採用されている。
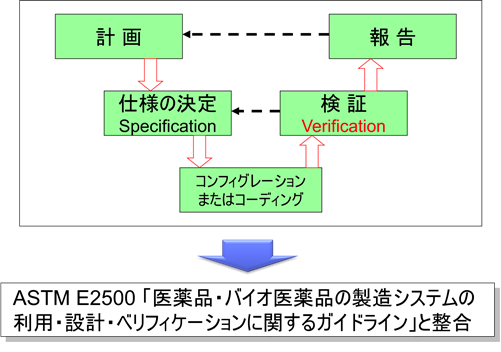
FDAの要請を受けたASTMは、2007年にASTM E2500 「Standard Guide for Specification, Design, and Verification of Pharmaceutical and Biopharmaceutical Manufacturing Systems and Equipment(医薬品・バイオ医薬品の製造システムの利用・設計・ベリフィケーションに関するガイドライン)」を作成した。
この翌年の2008年には、GAMPを主宰しているISPEが、ASTM E2500に整合させたGAMP 5 「A Risk-Based Approach to Compliant GxP Computerized Systems」を発行した。
GAMP 4とGAMP 5の違いは何といっても、タイトルからValidationという用語が消えたことである。
つまり、ASTM E2500に整合させ、Validationではなく、Verificationのガイダンスに変更したのである。このことはあまり知られていない。
一般的な仕様と検証のアプローチ(Specification & Verification Approach)
GAMP 4(英語版)における仕様と検証のアプローチ-いわゆるVモデルでは、検証の位置にValidationと記載されていた。
しかしながら、GAMP 5(英語版)においては、検証はVerificationに変更となっている。
ただし、GAMP 5(日本語版)では、どちらも検証のままとなっているため、その変化に気付かない。
GAMP 4においては、サプライヤが実施した活動を、製薬企業が再度Validationとして繰り返していた。これでは、コンプライアンスコストの無駄遣いである。
GAMP 5では、サプライヤが実施した活動を、製薬企業がVerification(確認)することとなった。これにより、サプライヤと製薬企業の作業の二重化が防げることとなったのである。
日本の企業の多くはこのことに気付いておらず、いまだにガチガチのValidation活動を実施しているのである。 品質保証は大切な活動ではあるが、過剰であってはならないのである。