医療機器基本要件基準とは
医療機器基本要件基準は、医療機器の安全性と有効性を確保するための重要な規制基準です。この基準は、以下の主要な特徴を持っている。
法的根拠と目的
医療機器基本要件基準は、薬機法(医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律)第41条第3項に基づいて厚生労働大臣が定めた基準である。この基準の主な目的は、医療機器の性状、品質、性能の適正を図ることである。
適用範囲
この基準は、すべての医療機器に適用される。つまり、承認申請や認証申請を行う際には、この基準への適合性を示す必要がある。
基準の構成
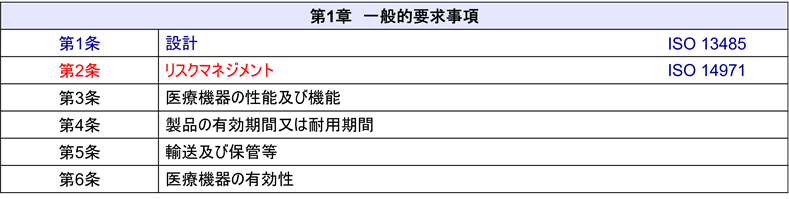
医療機器基本要件基準は、以下のような章立てで構成されている。
1. 第一章:一般的要求事項(必須)
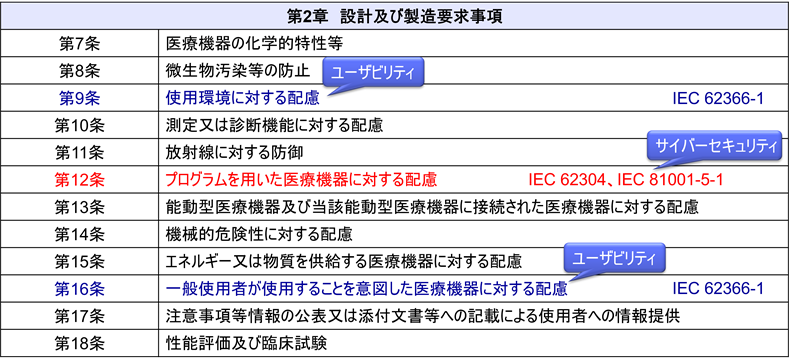
2. 第二章:設計及び製造要求事項(選択)
各章には、医療機器の設計、製造、性能、安全性に関する詳細な要求事項が記載されている。
主要な要求事項
基本要件基準には、以下のような重要な要求事項が含まれてる。
– 設計と製造における安全性の確保
– リスクマネジメント
– 医療機器の性能と機能の確保
– 化学的特性や生体適合性への配慮
– 微生物汚染の防止
– 測定・診断機能を持つ機器の精度と安定性
最近の改正
2023年4月1日から、サイバーセキュリティに関する新たな要件が第12条第3項として追加された。この改正により、特定の医療機器に対してサイバーセキュリティ対策が求められるようになった。
適合性の確認
製造販売業者は、基本要件基準への適合性を確認するためのチェックリストを使用することがでる。このチェックリストは、各要求事項に対する適合性を体系的に確認するためのツールとして活用されている。
医療機器基本要件基準は、医療機器の品質、有効性、安全性を確保するための重要な規制枠組みであり、製造販売業者はこの基準に適合した製品を市場に提供することが求められている。








